肝细胞水通道蛋白8(AQP8)介导的水转运促进小鼠胆汁稀释和防止胆结石形成
胆囊结石疾病发病率高,目前针对胆囊结石的药物治疗非常有限,有必要寻找新的药物靶点,开发具有普遍适用性的新药。尽管在人类和动物研究中,水通道蛋白-8 (aquaporin-8, AQP8)已被证实与肝胆汁形成以及与胆汁流量异常相关的肝脏疾病有关,但仍缺乏其参与胆汁分泌的直接证据。(Adv Sci | 灯盏乙素通过Pdk-Pdc轴改善线粒体葡萄糖氧化来拯救线粒体损伤—LIP-MS靶点鉴定(五))
2024年9月24日,南京中医药大学麻彤辉、大连医科大学马骁驰及石磊共同通讯在Journal of Hepatology(IF=26.8)在线发表题为“Hepatocyte Aquaporin 8-mediated Water Transport Facilitates Bile Dilution and Prevents Gallstone Formation in Mice”的研究论文,该研究发现肝细胞水通道蛋白8(AQP8)介导的水转运促进小鼠胆汁稀释和防止胆结石形成。通过构建AQP8调控的高通量筛选体系,对中医治疗胆结石的20种常用“利胆”中药进行筛选,从中药灯盏细辛中分离出药效活性小分子-灯盏乙素/野黄芩苷(Scutellarin)。野黄芩苷通过抑制AQP8的转录负调控因子HIF-1α与HSP90的相互作用,促进了HIF-1α的泛素化降解,从而上调AQP8基因表达,促进胆汁分泌,发挥利胆作用。这是第一个直接证明肝脏水通道AQP8在胆汁稀释和胆囊结石形成中起关键作用的研究。调节肝脏水转运可能为所有类型的胆石性疾病提供一种通用的治疗策略。

•AQP8介导正常胆汁分泌所需的高效水运输。
•AQP8缺乏导致胆汁浓缩,加速胆囊结石形成。
•上调AQP8可促进胆汁稀释,防止胆囊结石形成。
•调节肝脏水转运可能为治疗胆结石提供一种通用策略。
摘要
建立了各种转基因敲入和敲除小鼠模型,并通过免疫染色和免疫印迹评估了肝脏AQP8的表达,通过胆总管插管评估了肝脏胆汁分泌,通过喂食高脂致石饲料评估了胆固醇结石的形成,并通过筛选利胆中药的有机组分和生化表征确定了调节小分子。在大约50%的肝小叶的肝小管膜中发现了一种新的AQP8蛋白表达模式。与野生型小鼠相比,aqp8缺陷小鼠表现出肝胆汁形成受损,其特征是分泌的浓缩胆汁流速较低,胆汁脂质水平较高。AQP8-/-小鼠表现出加速的胆囊结石形成,aav介导的AQP8或AQP1的表达挽救了这一过程。此外,发现了一种小分子灯盏乙素,它可以在体外和体内上调肝细胞AQP8的表达。与AQP8-/-小鼠相比,灯盏乙素显著增加AQP8+/+小鼠胆汁流量,降低胆汁脂质浓度,并预防胆囊结石形成。分子研究表明灯盏乙素通过干扰HIF-1α与HSP90的相互作用,促进AQP8的转录负调控因子HIF-1α的泛素化和降解。AQP8在小鼠肝胆汁形成过程中具有促进水转运和胆汁稀释的作用,从而减轻小鼠胆囊结石的形成。小分子干预验证了肝细胞AQP8有望成为治疗胆结石的药物靶点。
1.AQP8定位于部分肝小叶的胆小管和紧密连接
为了研究AQP8在肝脏中的生理细胞分布,修改了基因组序列,使其在AQP8终止密码子之前包含一个三重Flag标签或一个GFP编码序列,从而生成了AQP8 c末端3xflag和GFP转基因敲入小鼠AQP8- flagtg和AQP8- gfptg(图1a和1B)。这种基因修饰使我们能够通过检测Flag和GFP信号来监测内源性AQP8的细胞分布。Western blot分析证实,在AQP8-FlagTg小鼠的肝脏中存在30 kDa和45 kDa的两个特异性Flag条带,以及在56 kDa和70 kDa的两个gfp阳性条带,而这些在WT小鼠中没有(图1 A-b和1B-b)。通过对AQP8- flagtg小鼠的肝切片进行免疫组化检查,首次观察到内源性AQP8表达在肝小叶中分布不均,这取决于中央静脉周围的阳性染色(图1 a ~ c,左)。高倍镜图像显示在泪小管结构中AQP8染色相对较强(图1 A-c,右)。在AQP8- gfptg小鼠中,直接观察了冰冻肝切片中AQP8的小管分布,这与f -肌动蛋白染色完美重叠(图1b -c,左下)。高倍荧光图像显示AQP8蛋白在泪小管膜和紧密连接处的明确定位(图1b -c,右下)。根据中央静脉计数,gfp阳性和gfp阴性小叶的数量分别约为49%和51%(图1 B-d),这与AQP8-FlagTg小鼠的观察结果一致。此外,基于GFP信号强度的FACS分析将原代肝细胞以几乎相同的百分比(分别为50.2%和49.8%)分为GFP和GFPhigh群体(图1 B-e)。这些观察结果为AQP8在肝脏中的细胞分布及其在肝胆汁形成中的潜在作用提供了新的见解。
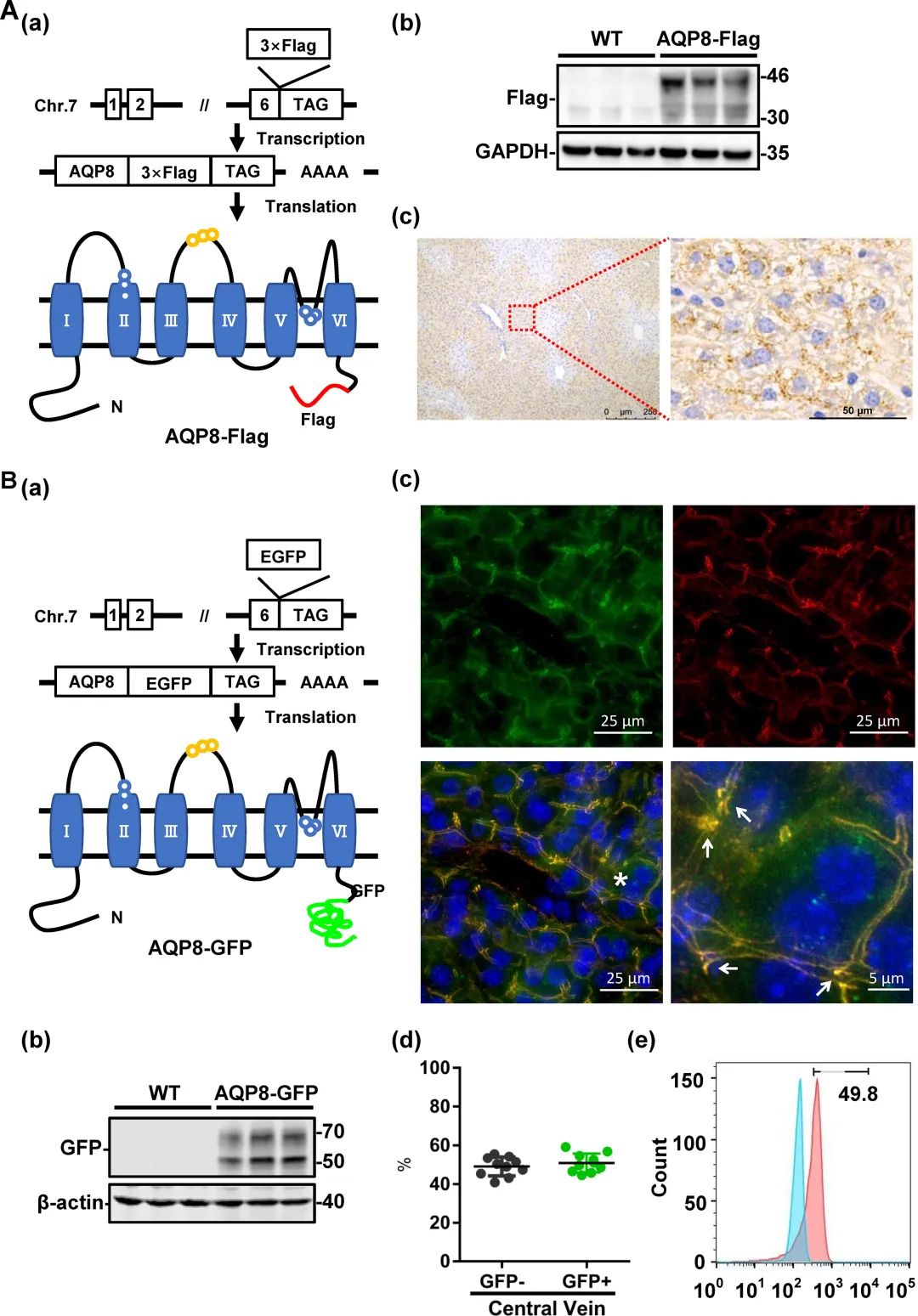
图1 AQP8在小鼠肝脏中的分布
2. AQP8是正常生理性胆汁分泌所必需的
为了检验AQP8促进肝胆汁形成的假设,使用两种方法评估胆汁流量:胆汁引流和胆管结扎模型(BDL)。在胆汁引流模型中进行了胆总管置管,以测量胆汁流速(图2A-a)。与WT同窝小鼠相比,AQP8-/-小鼠的胆汁流量显著减少(AQP8-/-小鼠的肝脏为66.7±6.4 μL/h/g,而WT小鼠的肝脏为100.9±2.8 μL/h/g)(图2 A-b&c)。与WT小鼠相比,AQP8-/-小鼠的胆汁渗透压显著增加(图2 A-c)。此外,AQP8-/-小鼠胆汁中的BA和CHO浓度分别升高了68.6%和61.2%(图2 A-c)。这些结果表明,AQP8缺失损害了胆汁分泌,导致胆汁脂质水平升高。为了研究AQP8-/-小鼠对胆盐刺激的反应,我们测定了静脉注射牛胆盐(50 mg/kg)后的胆汁流量和胆汁脂质排出量。胆盐刺激后,AQP8-/-小鼠和WT小鼠的胆汁流量差值进一步拉大(AQP8-/-小鼠肝脏分别为101.8±7.0 μL/h/g肝脏vs. WT小鼠肝脏分别为184.6±12.1 μL/h/g肝脏)(图2 A-d)。此外,与WT小鼠相比,AQP8-/-小鼠胆汁中的渗透压、BA和CHO显著增加(图2 A-d)。这些发现进一步表明AQP8-/-小鼠表现出胆汁分泌缺陷,特别是在存在胆盐刺激的情况下。
为了验证上述结果,还评估了小鼠清醒状态下BDL后胆囊内胆汁的体积(图2 B-a)。AQP8-/-小鼠在不同时间点(1 h、3 h和6 h)收集的胆囊胆汁体积显著低于WT小鼠(图2 B-b&c)。这些结果与小鼠麻醉后胆管插管模型的观察结果一致(图2a)。此外,AQP8-/-小鼠的胆囊胆汁中渗透压和胆汁脂质(BA、CHO和PL)水平显著升高(图2 B-d)。这些发现支持了AQP8在促进胆汁分泌中起重要作用的假设。
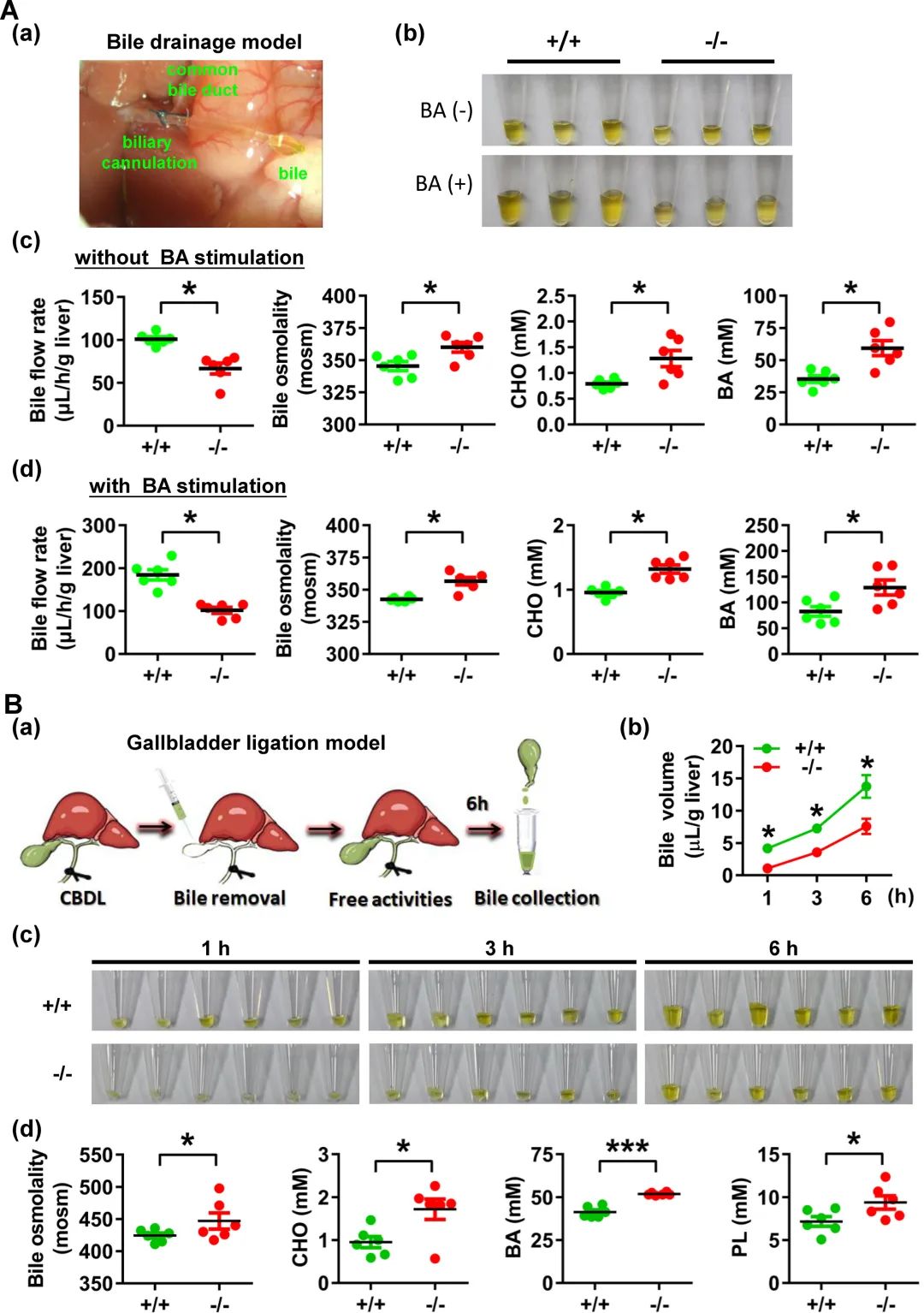
图2 AQP8缺乏对胆汁分泌的影响
3. AQP8基因敲除加速胆囊结石形成
为了研究AQP8在胆汁分泌缺陷中的病理意义,AQP8-/-和WT小鼠被喂食饲料或致石饲料(LD) 1周,3周和5周。与WT小鼠相比,AQP8-/-小鼠以时间依赖性方式表现出加速的胆囊结石形成(图3a)。偏振光图像分析显示,AQP8-/-小鼠的胆汁晶体比WT小鼠更多更大(图3a)。收集的胆囊结石在AQP8-/-小鼠中显著较重(2.51±0.33 mg对WT小鼠1.30±0.25 mg)(图3b)。60%的AQP8-/-小鼠由于充满的结石而发生胆囊梗阻(图3c)。这些结果清楚地表明,AQP8-/-小鼠在LD喂养后更容易形成胆囊结石。CHO、BA和PL是胆汁的主要成分,其失衡可导致结晶形成。采用傅里叶远红外光谱分析AQP8-/-和WT小鼠胆囊结石成分。令人惊讶的是,在AQP8-/-小鼠中,CHO红外吸收(2960、2935、2902和2867 cm-1)的透射率始终较低,表明胆石中CHO含量相对较高,而AQP8-/-小鼠和WT小鼠的BA和PL含量相当(图3d和3E)。此外,在LD喂养5周后,测定胆囊胆汁中胆汁脂质水平,以确定AQP8-/-和WT小鼠之间的差异。AQP8-/-小鼠的胆囊胆汁中CHO、BA和PL水平显著增加(图3f)。这些发现表明,AQP8缺乏导致胆汁脂质水平升高,加速了胆囊结石的形成。
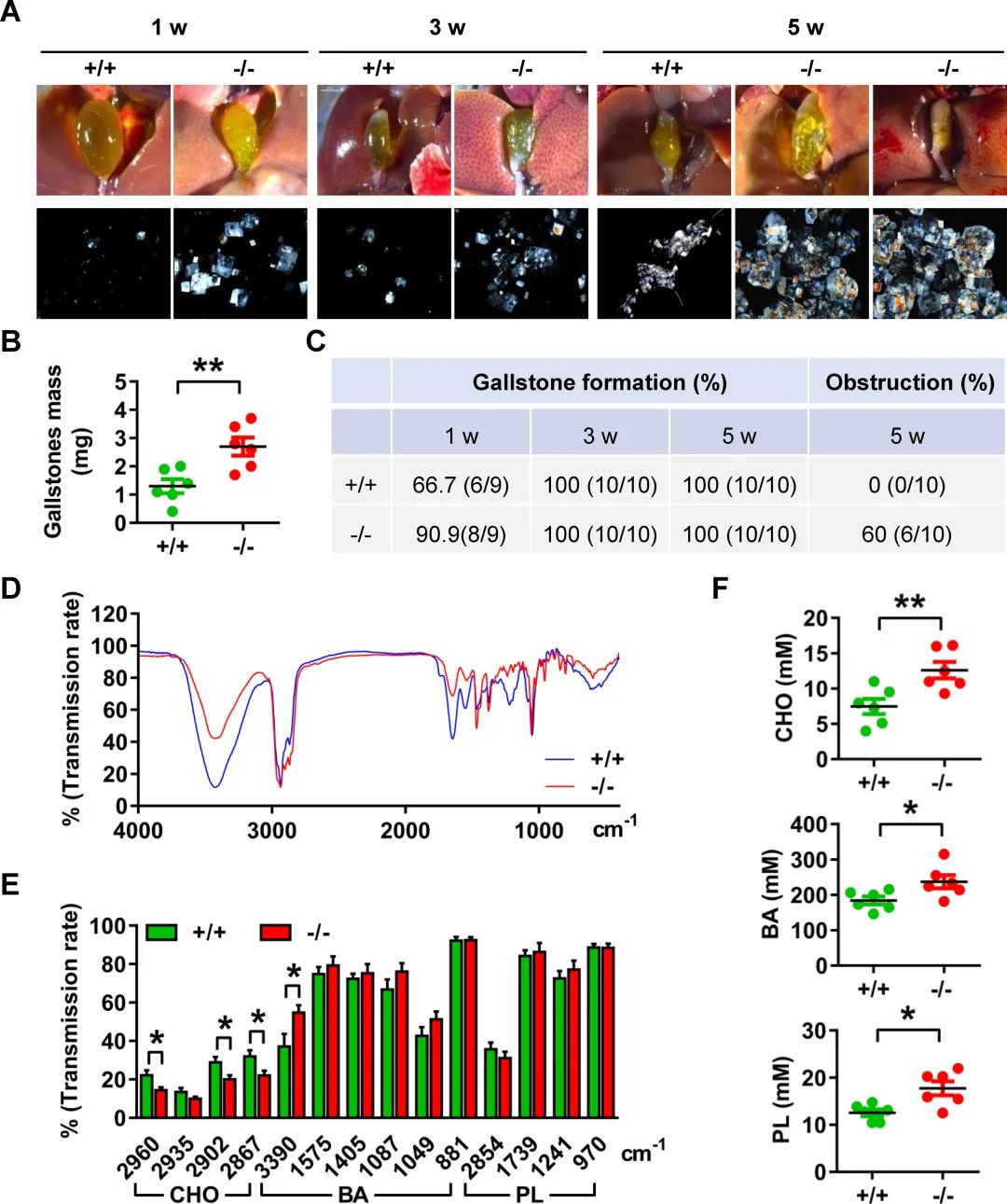
图3 Aqp8缺乏对胆囊结石形成的影响
4. 肝细胞特异性敲除AQP8可损害肝胆汁形成并加速胆囊结石形成
AQP8表达于肝细胞、胆管细胞和胆囊上皮。为了进一步揭示肝细胞AQP8在胆汁流动和胆囊结石形成中的作用,通过AQP8flox/flox和Alb-CreTg杂交产生了肝细胞特异性AQP8敲除小鼠(Q8ΔHEP)(图4a)。纯合子Q8ΔHEP小鼠显示,在分离的原代肝细胞中,正常AQP8转录减少约85%。对Q8ΔHEP小鼠的研究重现了AQP8-/-小鼠的主要缺陷,表现为胆汁流量减少,CHO/BA浓度增加(图4b),胆囊结石形成加速(图4c)。然而,我们注意到Q8ΔHEP和AQP8-/-小鼠之间的胆汁流量有显著差异,分别下降了15.6%和30.1%,这种差异可能与肝细胞中AQP8的不完全敲除以及AQP8介导的胆管上皮水转运可能参与有关。
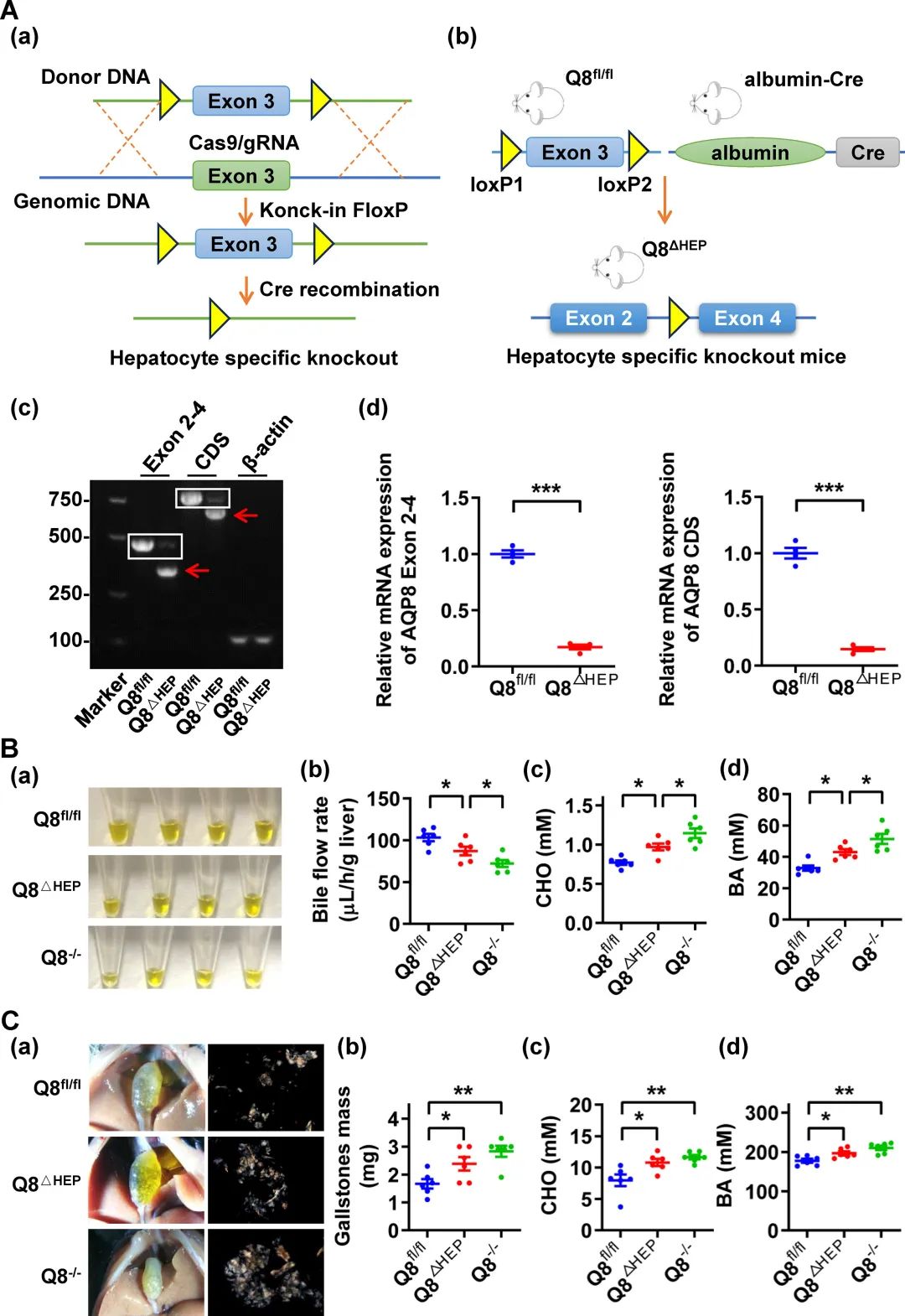
图4 肝细胞特异性AQP8敲除对小鼠胆汁分泌和胆囊结石形成的影响
5. 在AQP8-/-和野生型小鼠中,aav介导的肝脏AQPs表达可预防胆囊结石的形成
为了进一步研究AQP8在胆囊结石形成中的病理生理学意义,在肝细胞特异性TBG启动子下诱导aav介导的各种AQP同源物在肝脏中的表达。这一方法证明了GFP荧光与F-actin在实质膜的明确共定位,类似于内源性AQP8(图5 A-a&b)。此外,抗GFP抗体鉴定出分子量约为56 kDa和70 kDa的两条条带,证实外源性AQP8成功表达(图5 A-b)。我们的研究结果表明,在AQP8-/-小鼠中,外源性表达的AQP8显著减缓了胆囊结石的进展并减少了胆囊结石的质量(图5B)。在AQP8-/-小鼠中,aav介导的AQP1小管表达也显著减少了胆囊结石的质量,而aav介导的AQP5表达未能缓解胆囊结石的形成,因为AQP5蛋白定位于细胞内而非小管膜(图5A和B)。
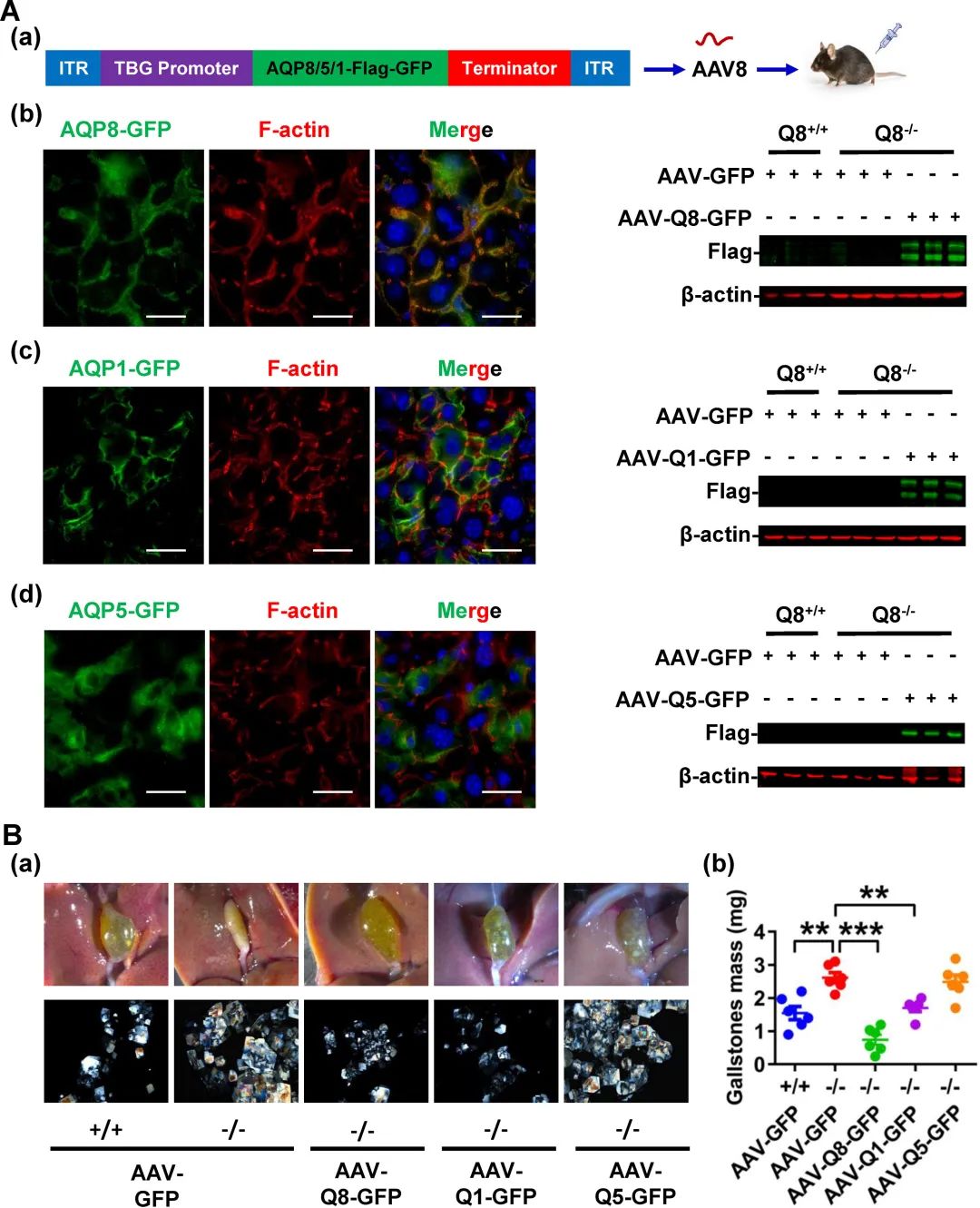
图5 肝脏AQP8、AQP1和AQP5表达对AQP8-/-小鼠胆囊结石进展的影响
6.从“利胆”中药中发现小分子AQP8诱导剂
中药促胆汁分泌、胆囊排空在临床上用于治疗胆囊结石、胆汁淤积、黄疸性肝炎及相关疾病的历史悠久。鉴于AQP8过表达在减少胆囊结石形成方面的潜在治疗益处,试图从利胆中药中识别可上调AQP8活性并有效治疗胆囊结石疾病的小分子。为了实现这一目标,进行了小鼠AQP8启动子荧光素酶报告基因检测,以筛选CTCMs(图6a)。CTCMs是根据其在中国药典中用于治疗肝胆疾病而选择的。在被测试的CTCMs中,灯盏细辛(C2)显示出显著的Aqp8诱导活性(增加1.6倍,图6 B)。采用主动示踪方法,根据其对AQP8转录活性的影响,分离和鉴定了灯盏细辛的有效化学成分。荧光素酶报告基因分析显示,在10 μg/mL的浓度下,Fr.10可以显著刺激AQP8启动子的活性(1.7-flod,图6 C)。最后,灯盏乙素,一种在灯盏花中大量发现的天然黄酮类化合物,以浓度依赖性方式显著增加AQP8启动子活性(图6d)。为了验证灯盏乙素对AQP8表达的调控作用,从AQP8- flagtg或AQP8- gfptg小鼠分离原代肝细胞,用不同浓度的灯盏乙素(0 ~ 10 μM)处理原代肝细胞。孵育24小时后,发现灯盏乙素使原代培养的肝细胞中的AQP8 mRNA和蛋白水平呈浓度依赖性增加,在10 μM灯盏乙素存在的情况下观察到大约2倍的上调(图6 E-6G)。CTCMs来源的灯盏乙素在体外可显著诱导肝脏AQP8的表达。
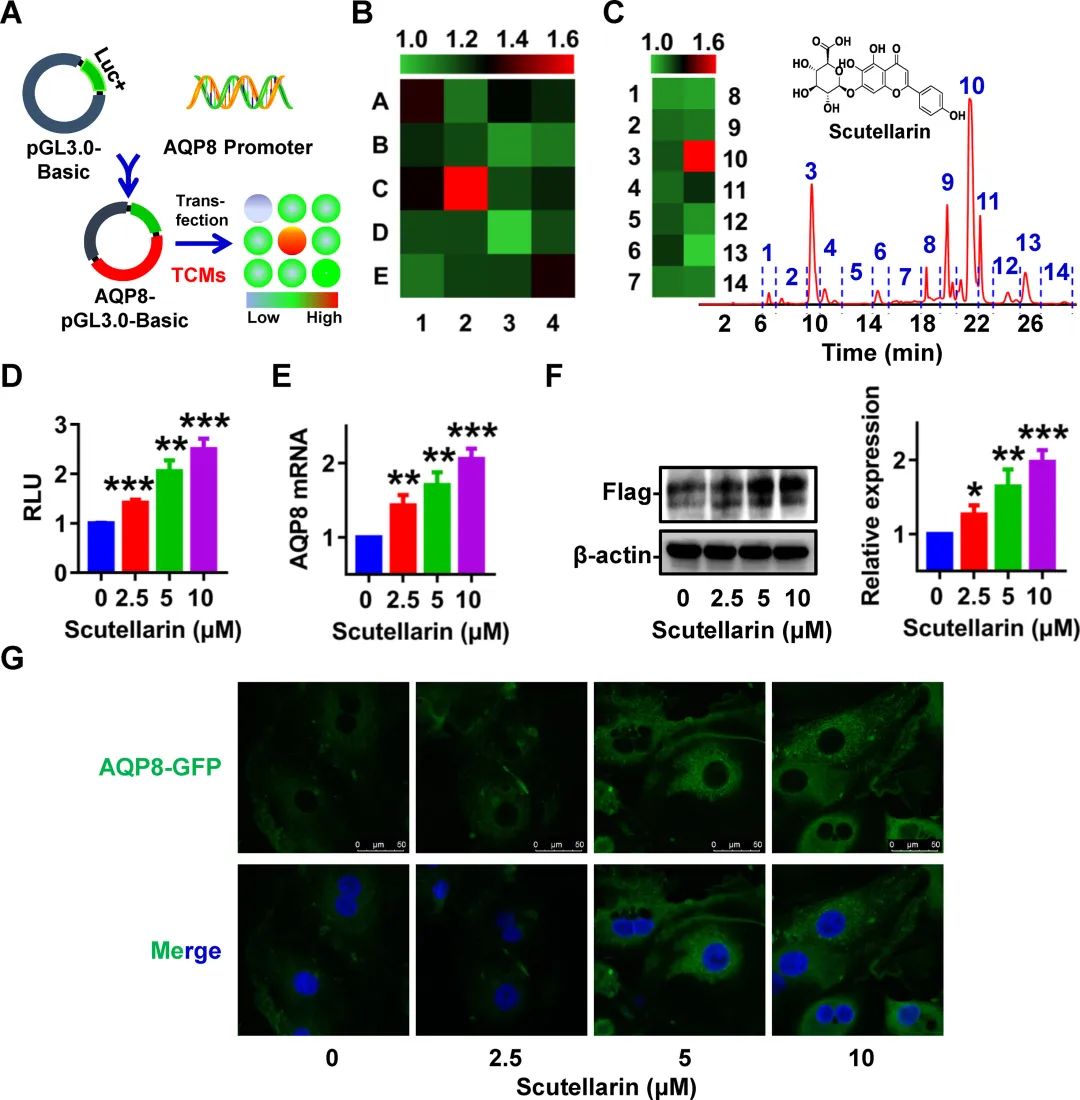
图6 黄芩素作为利胆中药中AQP8诱导剂的鉴定
7.灯盏乙素通过上调小鼠肝脏AQP8表达加速胆汁流动
为了确定灯盏乙素对小鼠AQP8表达和功能的体内影响,在WT和AQP8-/-小鼠中检测了给予灯盏乙素7天后肝脏AQP8表达水平和胆汁流量。首先,评估了经灯盏乙素处理或未处理的AQP8- flagtg小鼠的肝脏AQP8 mRNA和蛋白表达。结果显示,灯盏乙素治疗7天后,肝脏AQP8的mRNA和蛋白水平显著增加,表明灯盏乙素在体内上调了肝脏AQP8的表达(图7a和7B)。此外,通过监测灯盏乙素处理或未处理的WT和AQP8-/-小鼠的胆汁流量,评估灯盏乙素对胆汁分泌的潜在影响。在完全排空和回收胆汁6小时后,我们观察到灯盏乙素处理的WT小鼠的胆囊胆汁体积增加了37%。相反,在经灯盏乙素处理后的AQP8-/-小鼠中,没有观察到胆汁流量的显著差异,这表明胆汁流量的增加依赖于AQP8(图7c和7D)。此外,灯盏乙素处理后,WT小鼠的胆汁脂质(BA、PL和CHO)浓度显著降低(图7e)。然而,AQP8-/-小鼠的胆汁脂质未观察到显著变化,进一步支持野灯盏乙素促进胆汁分泌和稀释的AQP8依赖性作用。
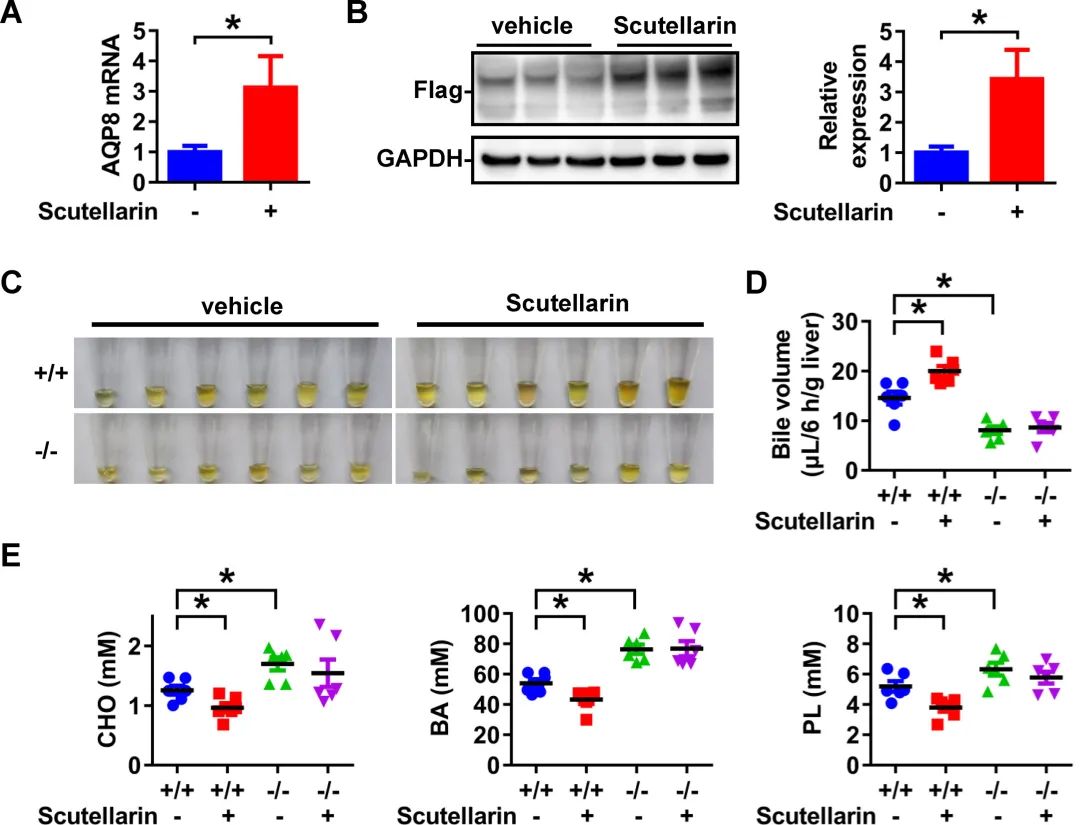
图7 灯盏乙素诱导野生型小鼠肝脏AQP8表达并加速胆汁排泄
8. 灯盏乙素可减轻致石饮食诱导的小鼠胆囊结石形成
为了评估灯盏乙素在治疗胆囊结石中的潜在疗效,WT和AQP8 - / -小鼠受到LD 5周有或没有给与灯盏乙素(10毫克/公斤)3周(图8)。发现灯盏乙素治疗可在LD饮食喂养的WT小鼠中诱导肝脏AQP8在mRNA和蛋白水平的表达(图8 B和8C),这证实了正常饮食喂养的WT小鼠的早期发现(图7 a和7B)。值得注意的是,灯盏乙素给药显著减少了WT小鼠的胆囊结石形成(图8 D)。胆汁晶体的发生率、大小和数量显著减少(图8 D)。此外,在WT小鼠中,灯盏乙素处理后,胆囊结石的干重下降了34%(图8 E)。然而,在AQP8-/-小鼠中,灯盏乙素处理对胆囊结石形成的影响很小(图8 E)。表明AQP8在灯盏乙素的治疗作用中是必需的。
为了深入了解灯盏乙素的作用机制,检测了胆汁排泄和溶质浓度。灯盏乙素治疗使WT小鼠的胆囊胆汁体积显著增加,并显著降低了包括CHO、BA和PL在内的胆汁脂质浓度(图8e)。这些观察结果提示,灯盏乙素通过增强AQP8的水转运来促进胆汁稀释。相反,AQP8-/-小鼠产生了体积较小、胆汁脂质水平较高的过饱和胆囊胆汁,并且对灯盏乙素治疗无应答(图8e)。这些发现进一步强调指出,灯盏乙素通过上调肝脏AQP8表达,稀释胆汁,从而改善ld诱导的胆囊结石形成。
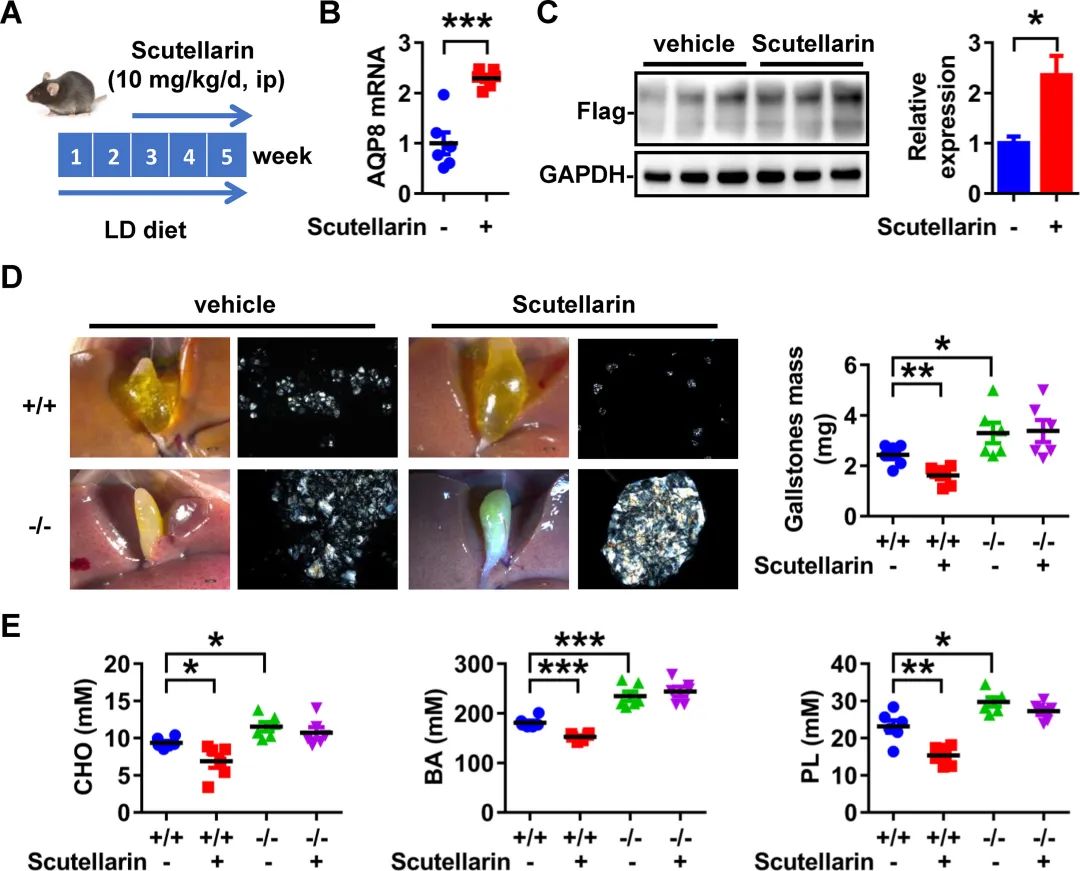
图8 灯盏乙素减轻了致石饮食诱导的小鼠胆囊结石
9. 灯盏乙素通过促进HIF-1α降解诱导AQP8表达
采用AQP8启动子pull-down实验结合串联质谱鉴定相互作用的蛋白,研究灯盏乙素诱导AQP8的分子机制。在接受或未接受灯盏乙素处理的小鼠肝匀浆中,我们在Aqp8启动子相关蛋白中观察到约120 kDa的明显条带(图9a)。随后,质谱分析在90-120 kDa范围内鉴定出180个蛋白质。其中,使用hTFtarget数据库发现8个蛋白是转录因子 (http://bioinfo.life.hust.edu.cn/ hTFtarget#!/)。DAVID进一步的功能注释表明,这些转录因子中的三个,STAT5α, STAT6和HIF-1α,与序列特异性DNA结合相关。通过蛋白质印迹法对这些鉴定的蛋白进行验证,只有HIF-1α与Aqp8启动子有显著的相互作用,并且在灯盏乙素处理后降低。另外的荧光素酶报告基因检测证实,在转染pc-HIF-1α后,Aqp8启动子活性被显著抑制(图9 B)。这些发现表明,核内HIF-1α作为转录因子直接与Aqp8启动子相互作用,并参与灯盏乙素诱导的Aqp8调控。
假设HIF-1α可能是灯盏乙素和AQP8之间的中介物。为了研究灯盏乙素、HIF-1α和AQP8之间的相互作用关系,评估了在灯盏乙素处理和未处理的小鼠肝脏和原代肝细胞中HIF-1α和AQP8的表达。在LD喂养的小鼠的肝脏中,灯盏乙素治疗显著增加了AQP8的蛋白表达(图8 C),但降低了HIF-1α的表达(图9 C),表明灯盏乙素可影响肝脏HIF-1α水平。进一步研究灯盏乙素对常氧和低氧原代肝细胞HIF-1α和AQP8表达的影响。在常氧条件下,灯盏乙素诱导AQP8蛋白表达,同时降低HIF-1α表达,尽管正常原代肝细胞的HIF-1α基础水平较低(图9 D和9E)。相反,低氧处理显著诱导原代肝细胞HIF-1α表达和核转位;然而,灯盏乙素的存在显著抑制了这些作用(图9d和9E)。灯盏乙素治疗也减弱了缺氧肝细胞中伴随的AQP8表达下降(图9d和9E)。相反,当用靶向HIF-1α的siRNA转染肝细胞时,灯盏乙素对AQP8的mRNA和蛋白水平无影响(图9f和9G)。这些结果表明灯盏乙素通过hif -1α依赖的方式诱导AQP8的表达。
为了研究灯盏乙素和HIF-1α之间的潜在相互作用,我们采用了免疫共沉淀,微尺度热电泳(MST)和对接试验。在肝细胞中,灯盏乙素导致HIF-1α的蛋白表达降低,而HIF-1α的mRNA水平不受影响(图9f和9G)。这一观察结果提示了一种转录后作用机制。值得注意的是,CHX抑制HIF-1α蛋白合成后,HIF-1α蛋白水平呈时间依赖性下降。灯盏乙素的存在加速了这一减少,而蛋白酶体抑制剂MG132可抵消这一减少(图9h和9I)。与灯盏乙素孵育后,HIF-1α的半衰期缩短了36.9%(图9 I)。这些结果强烈表明,灯盏乙素使HIF-1α蛋白不稳定。此外,灯盏乙素处理后HIF-1α的泛素化显著增加(图9j),直接表明灯盏乙素促进内源性HIF-1α降解。这些发现提供了令人信服的证据表明灯盏乙素是HIF-1α降解的有效诱导剂,从而调节AQP8的表达。
根据之前的一项研究,HIF-1α蛋白水平的调节涉及von Hippel Lindau (VHL)和HSP90的作用,它们分别调控蛋白酶体依赖的降解和稳定作用。有趣的是,研究发现灯盏乙素显著降低了HIF-1α和HSP90之间的关联(图9k),而不影响HSP90和VHL的蛋白水平,也不影响HIF-1α和VHL之间的相互作用。此外,MST分析证实灯盏乙素和HSP90之间有直接的相互作用,结合常数(Kd)为72.5±12.2 nM,而没有观察到与HIF-1α的结合(图9l)。
此外,分子对接实验还揭示了灯盏乙素与HSP90的相互作用模式。灯盏乙素与位于HSP90 A链的Glu679和Tyr627通过稳定的氢键结合在HSP90二聚体的c端界面上。这一结合干扰导致了Hsp90-HIF-1α相互作用的破坏(图9m);这些令人信服的发现表明,灯盏乙素通过干扰HSP90使HIF-1α不稳定,导致HIF-1α降解加速(图9 N)。因此,灯盏乙素诱导AQP8表达是通过促进HIF-1α降解实现的。
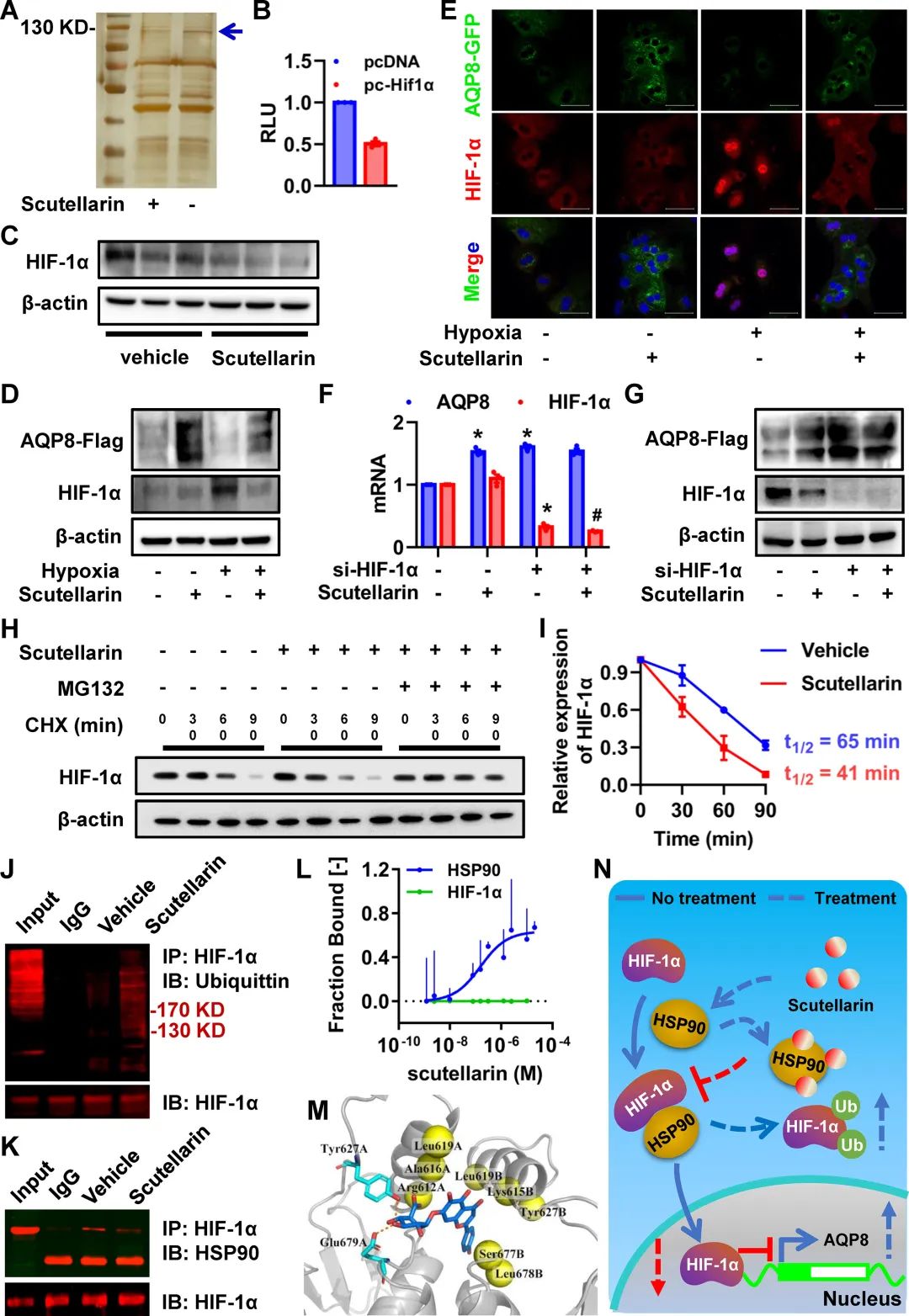
图9 灯盏乙素通过抑制HIF-1α与HSP90的相互作用,降解HIF-1α,诱导AQP8的表达
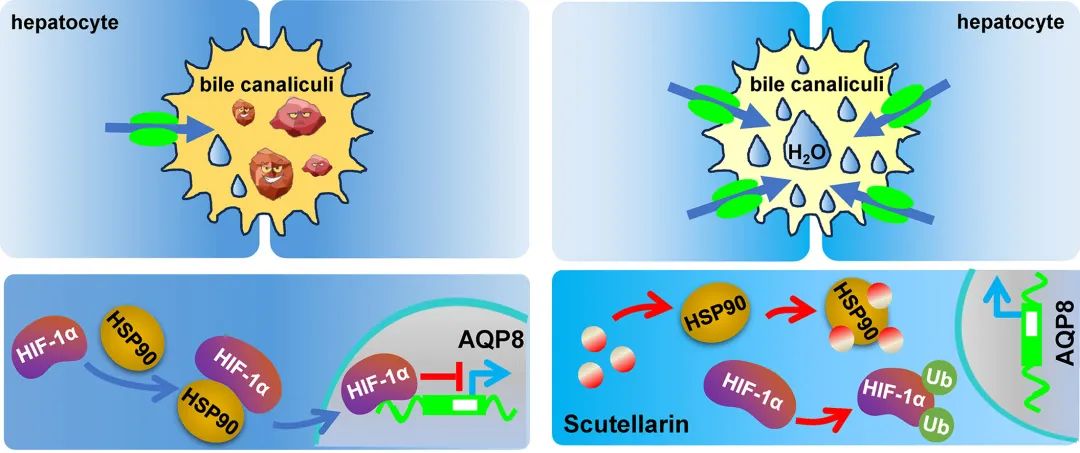
结论
我们的研究结果表明,在小鼠肝胆汁形成过程中,肝细胞AQP8在促进水转运和胆汁稀释中起重要作用,从而减轻胆结石的形成。小分子干预已证实肝细胞AQP8是治疗胆结石的一个有前景的药物靶点。调节肝脏水转运可能为所有类型的胆石性疾病提供一种通用的治疗策略。
Huo X, Yu Z, Zhao F, Chen Y, Chen P, Xing L, Qiao Y, Peng Y, Tian M, Zhou M, Wu F, Wang Y, Wang C, Tian X, Lv D, Zhang B, Shi L, Ma X, Ma T. Hepatocyte Aquaporin 8-mediated Water Transport Facilitates Bile Dilution and Prevents Gallstone Formation in Mice. J Hepatol. 2024 Sep 24:S0168-8278(24)02563-7. doi: 10.1016/j.jhep.2024.09.023.