Ferroptosis又一篇Adv Sci!中南大学刘勇团队:USP10通过去泛素化POLR2A抑制铁S亡!机制探究做的很到位~
小编是真的很佩服铁死亡这个方向,经久不衰啊,这么多细胞死亡方式就属它一直活跃在各大顶刊,研究热度只增不减~
7月2日,中南大学刘勇教授团队在顶刊Adv Sci上发表了一篇铁死亡方向的研究,思路非常清晰:
首先通过生物信息学分析和临床样本验证确定了目标基因(蛋白)USP10(一种去泛素化酶);接下来,通过体内外实验验证了该基因在头颈鳞癌中的作用;最后,进行一些列的机制探究,小编特别强调一下,这篇文章机制探究这部分做的很到位,最终确定了头颈鳞癌中USP10-POLR2A-SLC7A11轴在调控铁死亡中的关键调控作用。
这个信号轴是如何通过实验一步一步确定的呢?跟着小编一块看看吧~对铁死亡感兴趣的朋友的可以直接联系小编,这里有各种创新思路,基础、生信都可设计,专业团队主打一个全面、靠谱!

如何提出科学问题?
铁死亡已成为癌症治疗中诱导细胞死亡的一种新途径。去泛素化酶(DUBs)参与了癌症铁死亡,但其潜在机制尚未完全明了。目前,头颈部鳞状细胞癌(HNSCC)的治疗响应不佳,因此急需寻找新的分子靶点。而USP10作为DUBs的成员,已被发现与HNSCC的不良预后相关,但其在HNSCC铁死亡中的作用及机制尚未明确。
研究设计思路?

有哪些发现?
USP10 的表达及其在头颈部鳞状细胞癌中的临床意义
基于TCGA和GEO数据集(GSE42743 和 GSE41613)筛选出USP10,其高表达与患者队列中的不良预后紧密相关。通过免疫组化进一步发现HNSCC 中 USP10 蛋白的水平高于相应的癌旁非肿瘤样本,USP10 蛋白的高表达与总体生存率呈负相关。
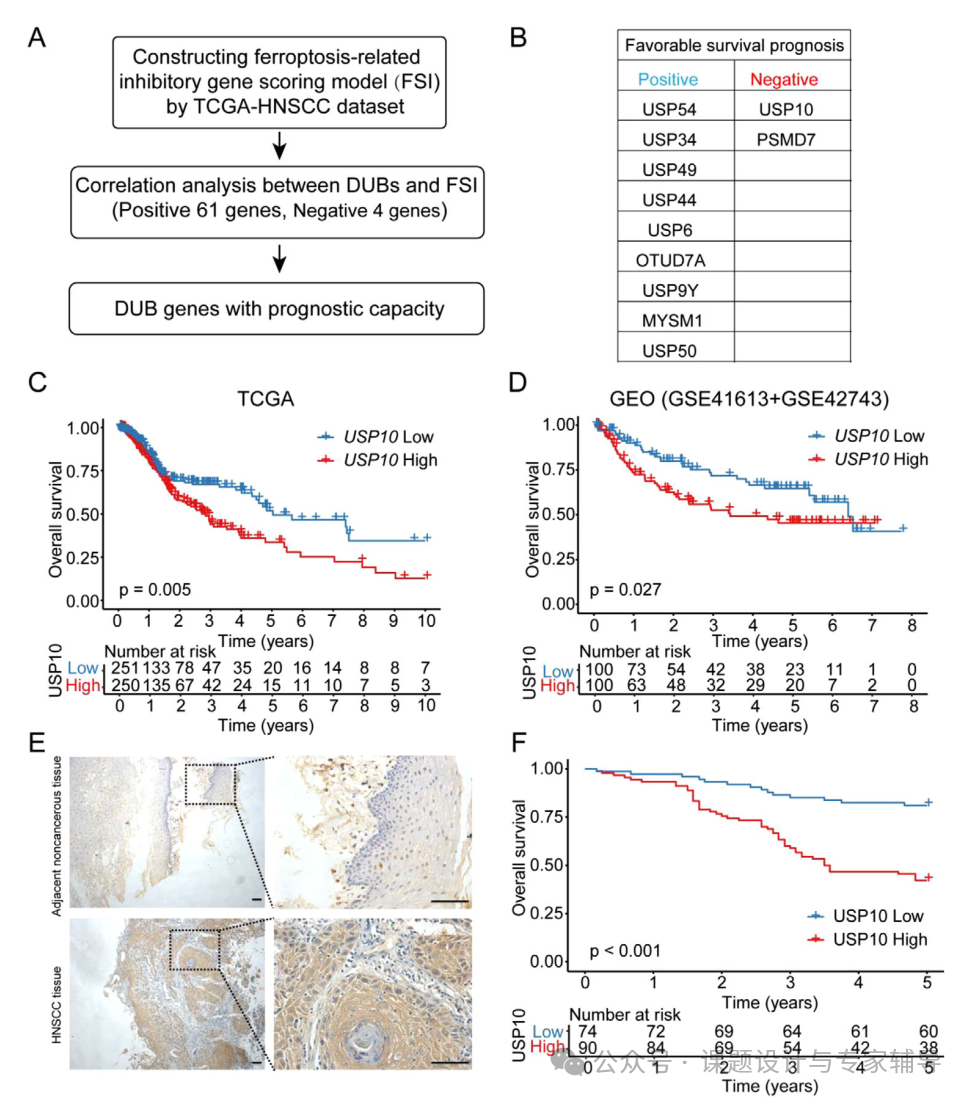
体内外功能验证
体外实验中,通过CRISPR技术敲除USP10,敲除USP10使 Fadu 和 SAS 细胞对铁死亡诱导剂的敏感性增加,表现为细胞活力下降、细胞死亡增加、脂质过氧化增强等,此外,这些效应可被铁死亡抑制剂逆转;
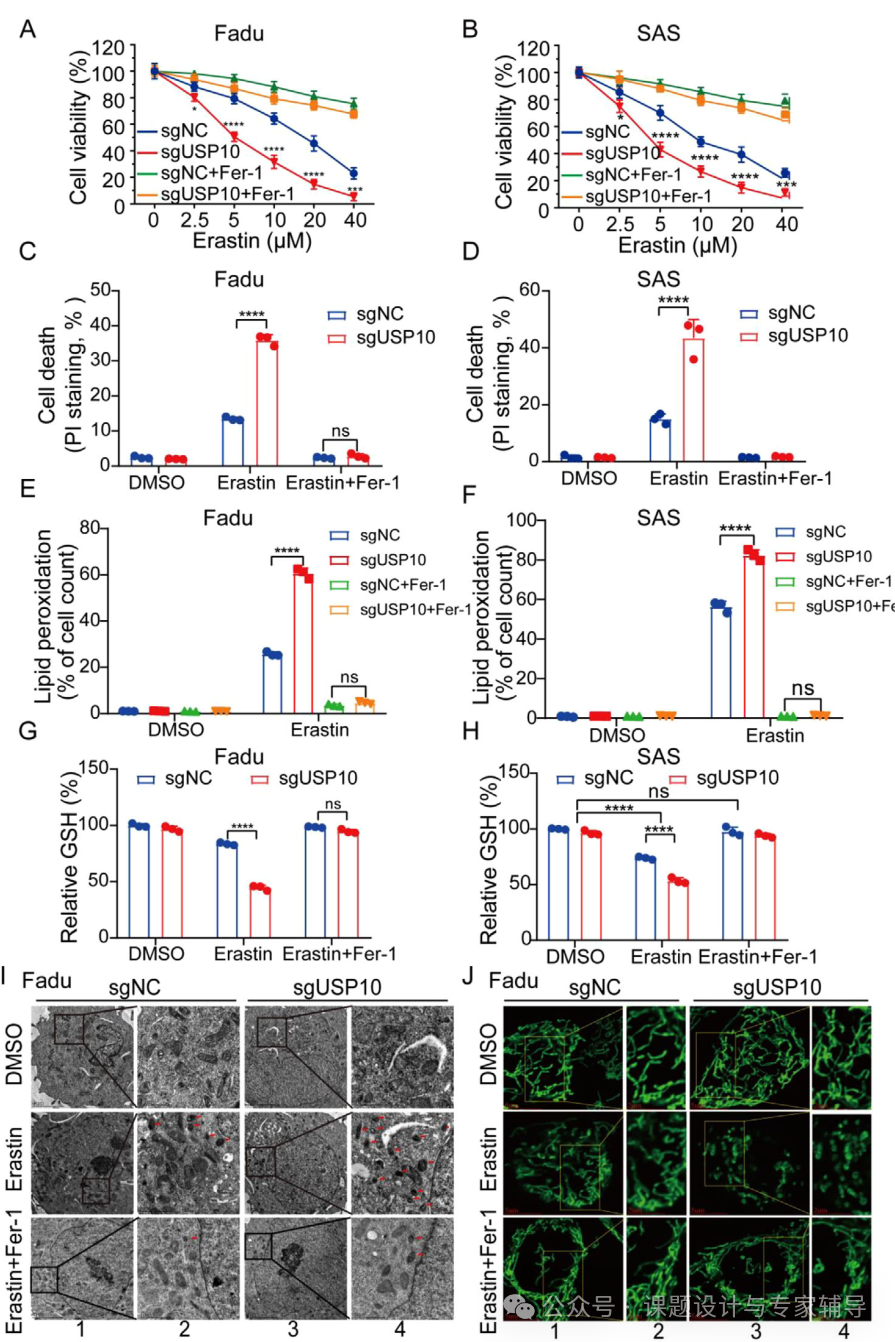
体内实验显示,USP10缺失联合铁死亡诱导剂 IKE 能协同抑制裸鼠移植瘤生长。体现在肿瘤生长模式、异种移植肿瘤以及肿瘤重量以及细胞增殖标志物 Ki67 和脂质过氧化标志物中。
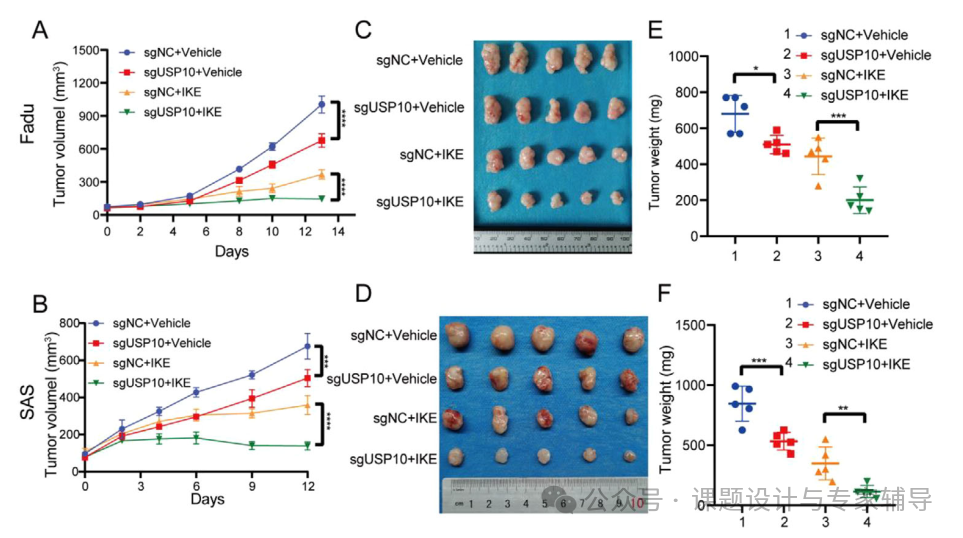
机制探究
1、对 USP10 缺失和对照的 Fadu 细胞进行RNA 测序,USP10 缺失显著降低 SLC7A11 的表达水平,并进行了mRNA和蛋白水平的验证;USP10 过表达使其升高,而 SLC7A11 敲除可逆转 USP10 过表达对铁死亡的抑制作用,说明 USP10 通过激活SLC7A11转录调控铁死亡。
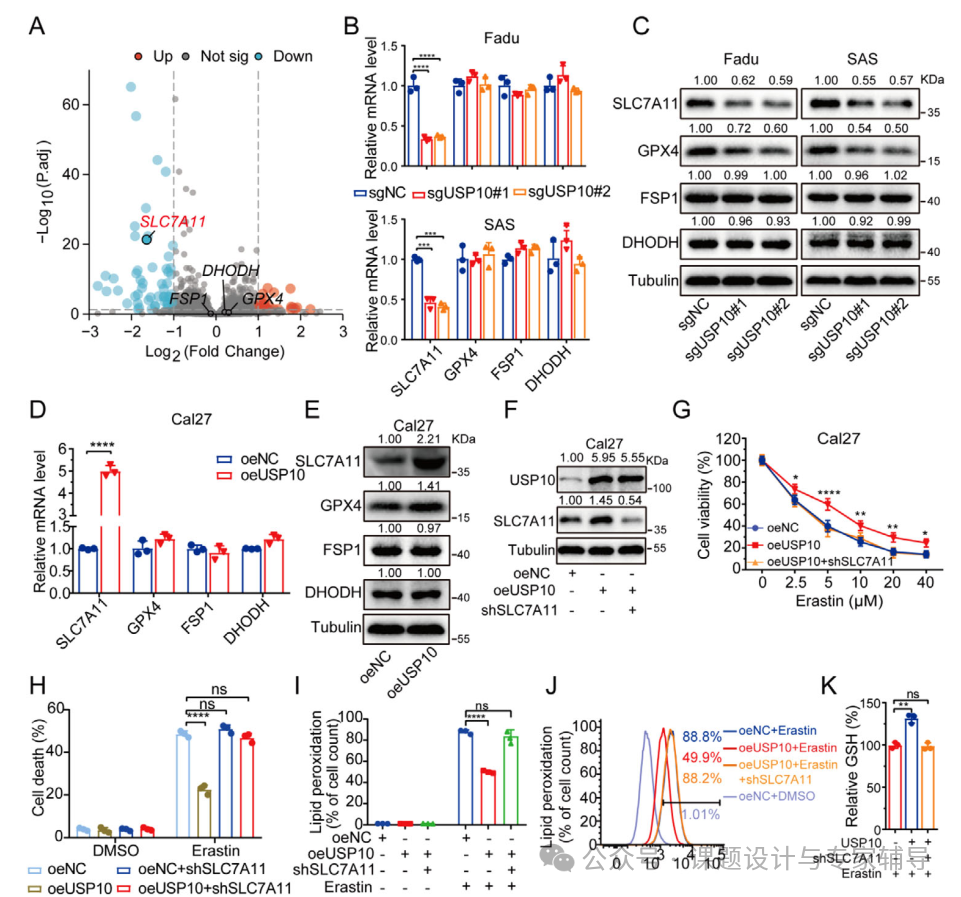
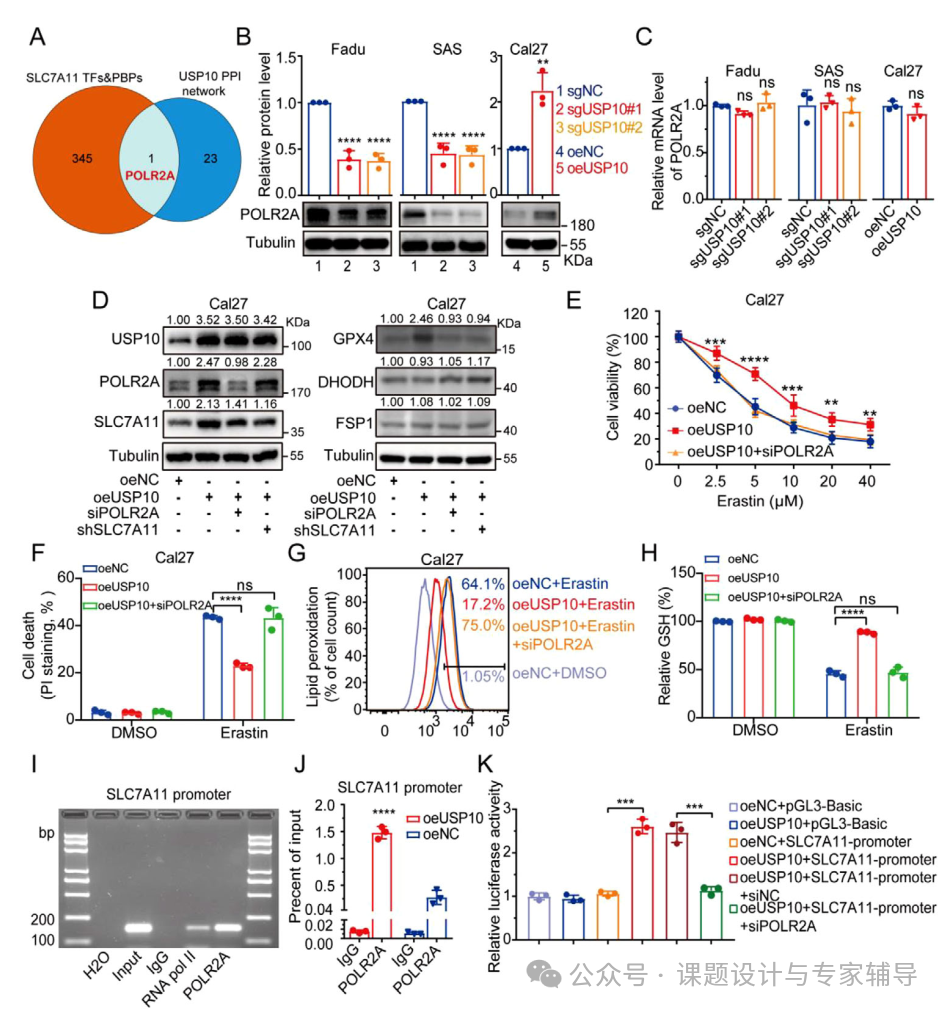
2、使用String预测 USP10 的互作网络,发现POLR2A 与 USP10 存在相互作用,USP10 敲除降低 POLR2A 蛋白水平(mRNA 无变化);POLR2A 敲除可逆转 USP10 过表达对 SLC7A11 的上调及对铁死亡的抑制,ChIP-PCR和荧光素酶报告质粒检测显示POLR2A 结合到 SLC7A11启动子区域并激活其转录。
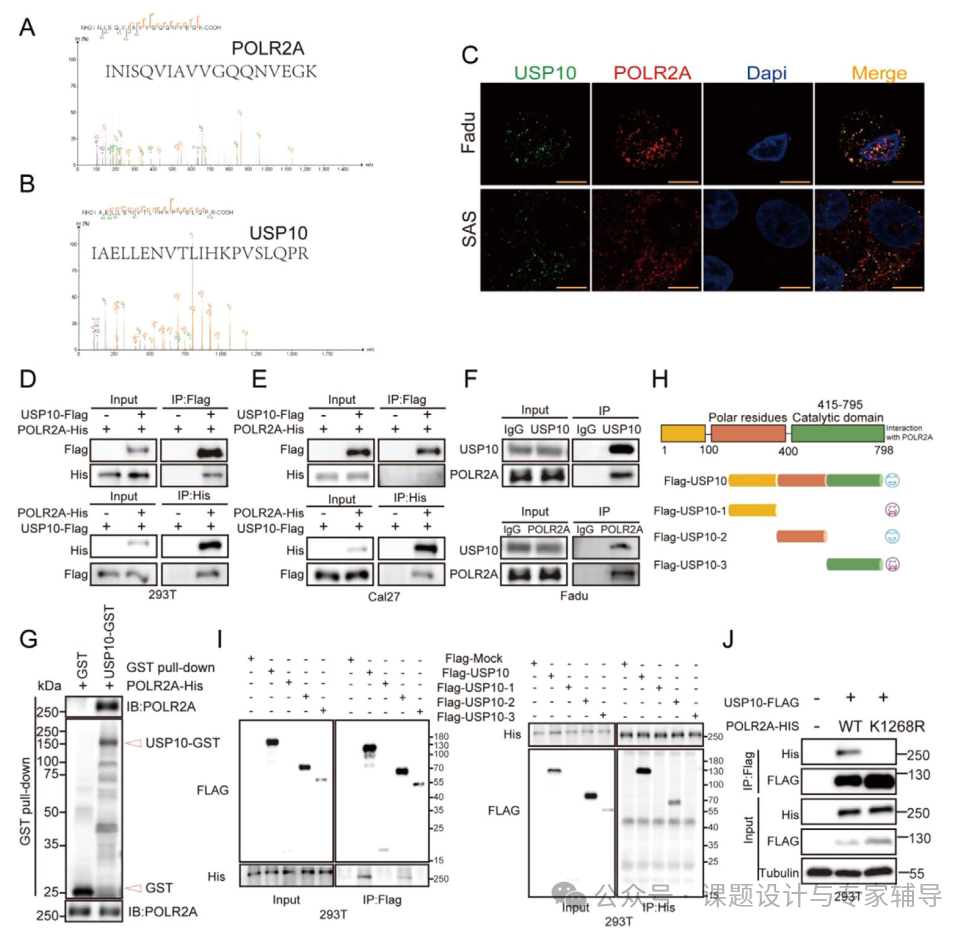
3、经过一些列实验(免疫荧光染色、CoIP等)证实USP10 与 POLR2A 之间存在直接相互作用。USP10通过其去泛素化活性去除 POLR2A 的 K48 和 K63 连接的泛素链,抑制其泛素化降解,从而维持 POLR2A 的蛋白稳定性。
小编点评
该研究证实USP10 是一种能抑制铁死亡的因子,具有治疗潜力和临床价值,并且可以作为预后指标使用。这项研究为 USP10-POLR2A-SLC7A11 轴在癌症铁死亡中的作用提供了有力证据。