IF 14.6|恭喜北中医博士一作发顶刊!天然产物抑制HIF1a/p300/HMGB1信号通路减轻铁SW,我的课题有着落了!

期刊:Acta Pharmaceutica Sinica B。
发表时间:202504
研究主旨:旨在探究 Acteoside(ACT)是否通过靶向 PCBP2 抑制肝细胞铁死亡,并减轻肝缺血再灌注损伤(HIRI)。文章发现,ACT通过促进PCBP2稳定 System Xc及抑制HIF1α/p300/HMGB1信号轴,从而改善肝细胞铁死亡和HIRI
研究思路

机制图解
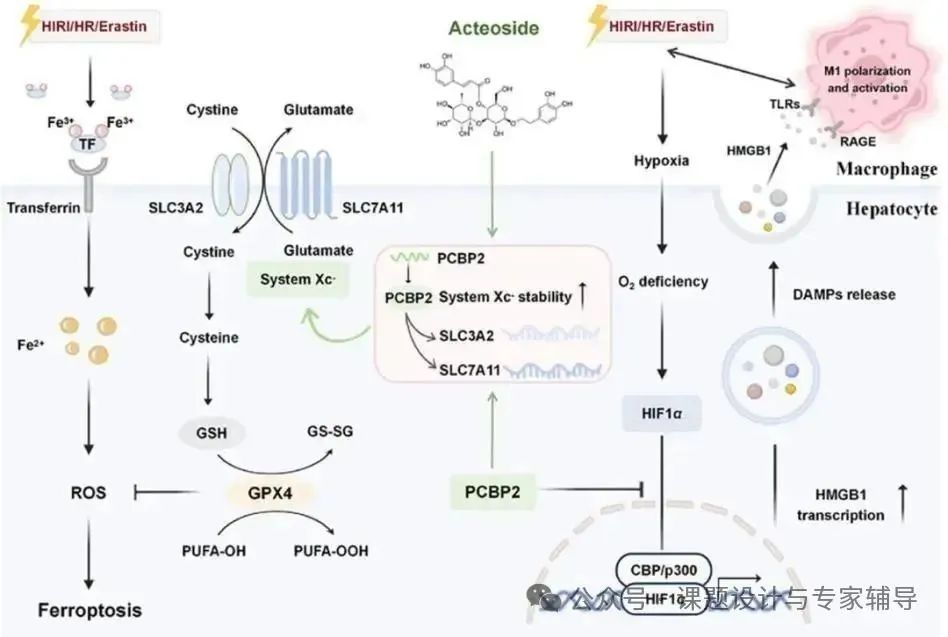
结果展示
一、ACT对HIRI的保护作用与抑制铁死亡相关
肝功能与组织学改善:ACT可降低HIRI小鼠血清中AST、ALT及MDA水平,升高SOD水平,减轻肝组织缺血及炎症浸润。
转录组学分析:HIRI相关差异基因富集于铁死亡通路,ACT处理显著下调脂质过氧化等铁死亡相关通路
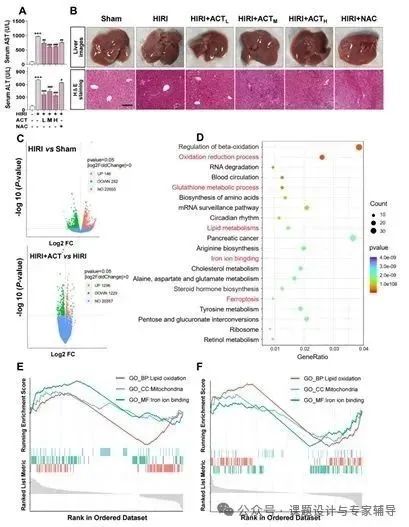
二、ACT上调缺血缺氧肝细胞中的PCBP2
表达验证:HIRI下调肝组织及原代肝细胞中PCBP2,ACT处理后显著上调其mRNA和蛋白表达。
氧化应激关联:ACT减少HR或erastin诱导的AML 12细胞ROS生成,恢复PCBP2表达。
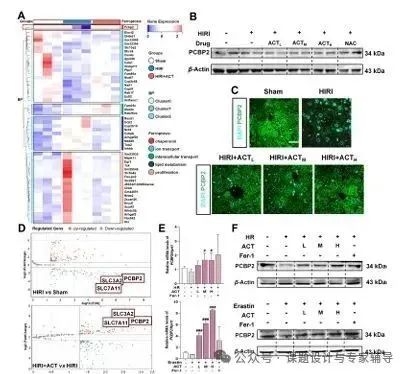
三、ACT通过PCBP2维持System Xc稳定性
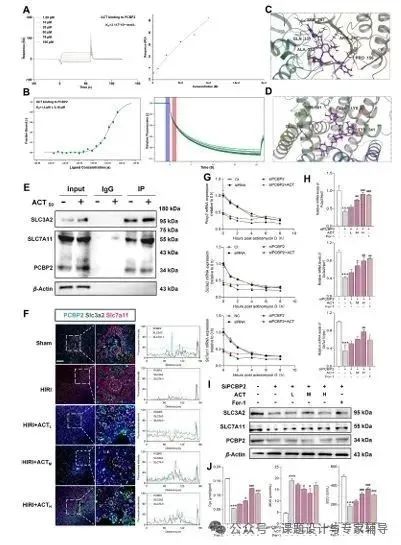
功能与表达调节:ACT促进PCBP2与SLC3A2/SLC7A11的正相关表达,增强其共定位,恢复Cys和GSH水平。
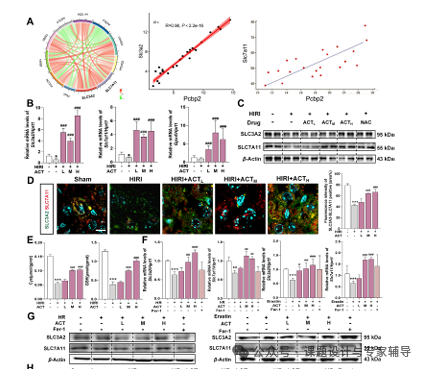
分子机制:ACT与PCBP2直接结合,增强PCBP2与System Xc⁻的相互作用,稳定SLC3A2/SLC7A11的mRNA。

该研究发现HIRI中,肝细胞铁死亡与PCBP2下调相关,PCBP2下调破坏System Xc⁻稳定性,激活HIF1α/p300/HMGB1信号轴,促进M1巨噬细胞募集。Acteoside(ACT)通过结合PCBP2,稳定System Xc⁻并抑制上述信号轴,减轻铁死亡及HIRI,肝细胞特异性敲低PCBP2可削弱ACT疗效。
可以扩展的方向:
1.PCBP2调控网络拓展:未来可以基于RNA-seq数据,结合ChIP-seq分析PCBP2结合的mRNA靶点,构建其与铁死亡、炎症相关基因的调控网络,通过GO/KEGG验证关键通路,筛选关键分子。
2.多组学联合分析:可以整合转录组、蛋白质组和代谢组数据,利用生信工具关联差异分子与代谢通路,结合分子对接预测ACT与PCBP2的结合位点及功能影响。
整体来看,这篇文章无论是从选题还是思路都很值得大家借鉴,篇幅有限小编就不一一展开了,感兴趣的可以找小编聊聊,尤其是中医药领域中的小伙伴们,想要节省时间的,可以直接找小编定制方案和生信分析哦~